QUÍMICA BÁSICA
I
TEMAS
01.-ESCRIBE EN TU PROYECTO EL TEMARIO DE ESTE PROYECTO.

OBSERVA LOS VIDEOS Y ANALIZA LA INFORMACIÓN (SIN ACTIVIDAD)
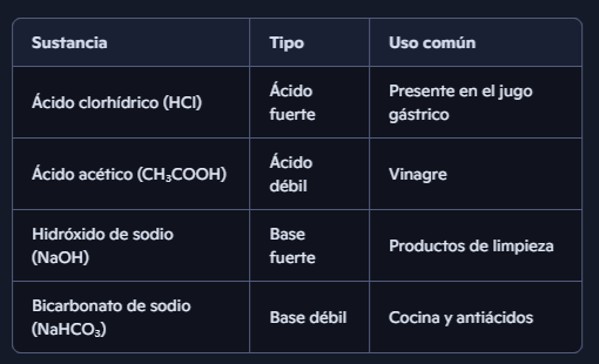
02.-ESCRIBE EN TU PROYECTO EL SIGUIENTE RESUMEN, ASI COMO TAMBIÉN EL CUADRO DE EJEMPLOS.
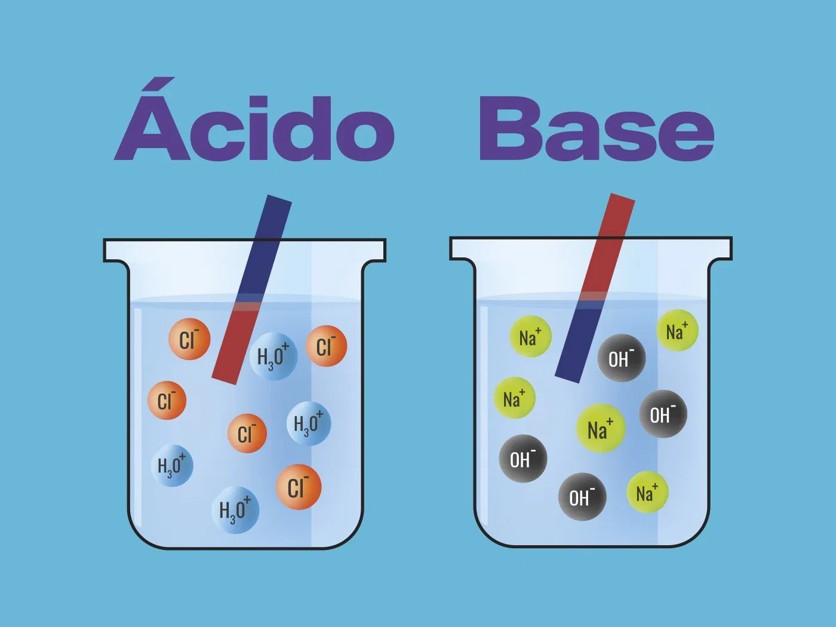
Los ácidos y las bases son sustancias químicas fundamentales: los ácidos se caracterizan por liberar protones (H⁺) y las bases por captarlos o liberar iones hidroxilo (OH⁻). Su comportamiento se mide con el pH: menor a 7 indica acidez y mayor a 7 indica basicidad.
Conceptos
Ácido (según Arrhenius): Sustancia que en solución acuosa libera iones de hidrógeno (H⁺).
Ejemplo: HCl (ácido clorhídrico) → se disocia en H⁺ y Cl⁻.
Base (según Arrhenius): Sustancia que en solución acuosa libera iones hidroxilo (OH⁻).
Ejemplo: NaOH (hidróxido de sodio) → se disocia en Na⁺ y OH⁻.
Teoría de Brönsted-Lowry:
Ácido = donador de protones.
Base = aceptador de protones.
Teoría de Lewis:
Ácido = acepta un par de electrones.
Base = dona un par de electrones.
Propiedades Principales
Ácidos:
Sabor agrio (ejemplo: limón, vinagre).
Corrosivos en altas concentraciones.
Cambian el papel tornasol a rojo.
pH menor a 7.
Bases:
Sabor amargo y tacto jabonoso.
Pueden ser cáusticas.
Cambian el papel tornasol a azul.
pH mayor a 7.
¿QUE PASA QUIMICAMENTE EN NUESTRO CUERPO?
En nuestro cuerpo ocurren procesos químicos constantes que permiten la vida. Estos procesos se llaman reacciones metabólicas y son responsables de transformar los alimentos en energía, reparar tejidos y mantener el equilibrio interno.
Principales Procesos Químicos en el Cuerpo
Digestión:
Los ácidos del estómago (como el HCl) descomponen los alimentos.
Las enzimas (proteínas especializadas) transforman carbohidratos en glucosa, proteínas en aminoácidos y grasas en ácidos grasos.
Respiración celular:
La glucosa se combina con oxígeno en las células para producir energía (ATP).
Reacción general:
C6H12O6+O2→CO2+H2O+energıˊa (ATP)
Homeostasis (equilibrio químico):
El cuerpo regula el pH de la sangre (alrededor de 7.4).
Los riñones y pulmones eliminan sustancias de desecho (urea, CO₂).
Síntesis de moléculas:
El cuerpo fabrica hormonas, neurotransmisores y proteínas a partir de moléculas más simples.
Ejemplo: síntesis de hemoglobina para transportar oxígeno.
Defensa inmunológica:
Los anticuerpos son proteínas que reconocen y neutralizan sustancias extrañas.
Se generan mediante complejas reacciones químicas en las células inmunes.
Ejemplo Cotidiano
Cuando comes pan:
Se convierte en glucosa durante la digestión.
La glucosa entra a las células.
Con oxígeno, se transforma en energía (ATP).
El exceso se guarda como grasa o glucógeno.
En resumen, somos un laboratorio químico viviente: cada segundo miles de reacciones ocurren para mantenernos con energía, reparar daños y defendernos de enfermedades.
CONCENTRACIÓN DE MEZCLAS QUIMICAMENTE
La concentración de mezclas en química se refiere a la cantidad de soluto (la sustancia disuelta) presente en una determinada cantidad de disolvente o de solución. Es una forma de expresar qué tan "fuerte" o "diluida" está una mezcla.
Formas de expresar la concentración

Partes por millón (ppm) / Partes por billón (ppb): Se usan para concentraciones muy pequeñas, como contaminantes en agua o aire.
Ejemplo cotidiano
El jugo que preparas con agua y azúcar:
Si agregas mucha azúcar, la concentración aumenta.
Si agregas más agua, la concentración disminuye.
La concentración química indica la proporción de soluto en una mezcla y se puede expresar de distintas maneras según la precisión que se necesite.
OBSERVA LOS SIGUIENTES VIDEOS Y ANALIZA LA INFORMACIÓN (SIN ACTIVIDAD)
ENTREGA TU PROYECTO DANDO CLIC EN LA IMAGEN DE ABAJO👇👇👇👇
Si deseas comunicarte con tu asesora por favor manda mensaje por WhatsApp al número 7206277984
Correo electrónico entregomiproyecto2@gmail.com
Asesora de inscripción ..... Liliana Pérez Hernández Tel. 55 5470 4044
M.S. CORPORATIVO PARA LA FORMACIÓN DE PROFESIONISTAS A.C
No dejes de avanzar, lo tienes en tus manos
Tú decides como será tu futuro.